Los estudios clínicos nos ayudan a aprender más acerca de las formas de prevenir o tratar afecciones médicas. La investigación debe demostrar que un medicamento en estudio es seguro y eficaz antes de que su uso pueda aprobarse. Sin estos estudios de investigación clínica y los voluntarios que participan en ellos, la medicina moderna no existiría.
Primero comprobamos una vacuna o medicamento en estudio con un pequeño grupo de participantes en un estudio clínico para entender su seguridad. Si la seguridad es aceptable, entonces comprobamos la vacuna o medicamento en estudio con un grupo más grande de personas para comprender la eficacia y seguimos observando la seguridad. Esta serie de estudios clínicos se desarrolla en cuatro fases principales.
Las cuatro fases de los estudios clínicos
1
Como participante en un estudio clínico de fase 1, ayudará a los investigadores a comprender la seguridad de un medicamento en estudio. Es posible que deban realizarle exámenes clínicos y análisis de laboratorio frecuentes y le pedirán que informe cualquier problema o efecto secundario.


2
Al inscribirse en un estudio clínico de fase 2, ayudará a los investigadores a entender mejor la eficacia con la que el medicamento en estudio puede actuar sobre la afección médica que se está estudiando y los efectos secundarios que pueden ocurrir.


3
En un estudio clínico de fase 3, formará parte de un grupo más grande de personas que padecen la afección médica que se está estudiando. Su participación ayuda a los investigadores a determinar si el medicamento en estudio es seguro y eficaz para las personas que tienen la afección médica que se está estudiando.


4
Incluso después de que se apruebe la administración de los medicamentos, puede seguir participando en estudios clínicos a largo plazo diseñados para comprender mejor los efectos del medicamento aprobado a lo largo del tiempo.


 Presentación
Presentación
 Revisión
Revisión
 Aprobación
Aprobación
 Disponible para los Pacientes
Disponible para los Pacientes
Cómo se diseñan los estudios clínicos
Protocolo
Los estudios clínicos comienzan con un protocolo. Un protocolo de estudio clínico es un plan detallado que explica el objetivo del estudio clínico y cómo se llevará a cabo. Incluye:

la duración del estudio clínico

información sobre quiénes pueden participar

los medicamentos en estudio, los procedimientos y las pruebas del estudio clínico

el seguimiento, el manejo y el informe de los efectos secundarios

el calendario de actividades del estudio

las reglas que deben seguirse
El protocolo también describirá si el estudio clínico:
- utiliza un método de asignación llamado randomización
- está controlado
- utiliza enmascaramiento
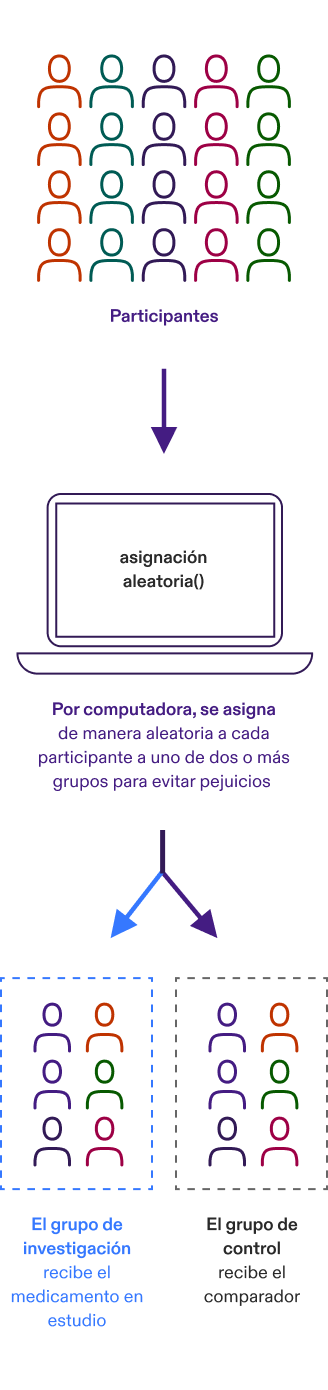
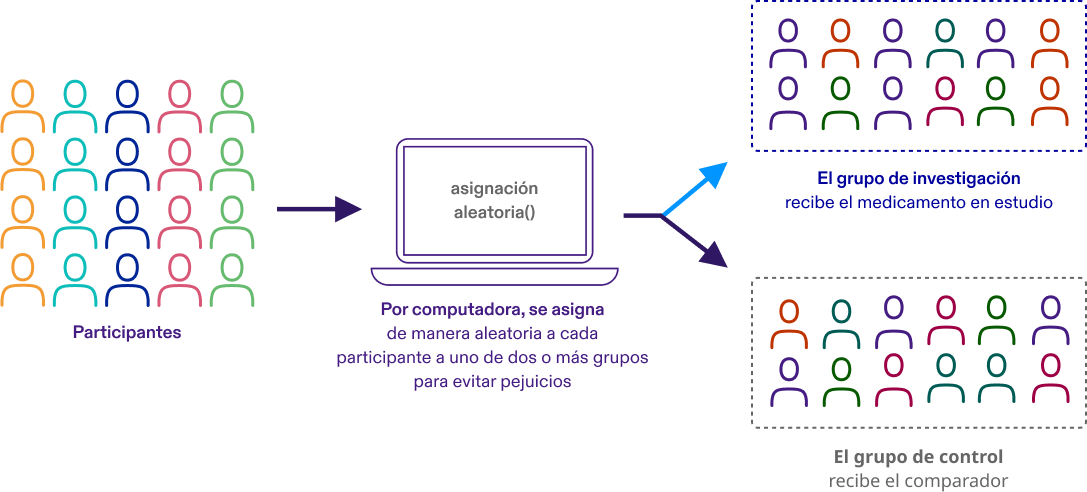
Randomización
Los participantes se asignan a diferentes grupos de tratamiento en un estudio clínico mediante un proceso llamado randomización. La randomización significa que los participantes se asignan a un grupo de tratamiento al azar (como cuando se lanza una moneda al aire) en lugar de por elección.
La randomización ayuda a evitar los prejuicios en un estudio. Por ejemplo, ayuda a asegurar que no todas las personas del mismo sexo o de la misma edad estén asignadas al mismo grupo de tratamiento.
Estudio controlado
Un estudio controlado es un estudio clínico que incluye un grupo de comparación (control). En los estudios clínicos controlados, los participantes se colocan en grupos que reciben el medicamento en estudio o un medicamento de comparación (llamado “comparador”). Aprendemos sobre la eficacia y seguridad del medicamento en estudio comparando las experiencias de los participantes que reciben el medicamento en estudio con aquellos que reciben el comparador.
Un ejemplo común de un comparador es el “tratamiento de referencia”, es decir, el tratamiento establecido que se utiliza actualmente para una afección médica.
En un estudio controlado “con doble enmascaramiento”, se utilizan placebos para evitar que el participante y el equipo del estudio sepan si el participante está recibiendo el medicamento en estudio o el comparador. A la vista, el medicamento en estudio y el placebo son iguales, pero el placebo no contiene ningún principio activo (es decir, ingrediente activo que pueda tratar o prevenir una afección). A continuación, encontrará más información sobre los estudios con enmascaramiento y doble enmascaramiento.
Estudios clínicos con enmascaramiento único o enmascaramiento doble
Los estudios clínicos pueden tener enmascaramiento único o enmascaramiento doble.
En un estudio con enmascaramiento único, los participantes no saben si están recibiendo el medicamento en estudio o el placebo, pero los investigadores sí lo saben.
En estudios con enmascaramiento doble, ni los participantes ni los investigadores saben si los participantes están recibiendo el medicamento en estudio o el placebo. (Si es necesario, por ejemplo, por motivos de seguridad, los investigadores pueden averiguar lo que un participante ha recibido).
En los estudios clínicos se utiliza el enmascaramiento para ayudar a evitar el prejuicio. De esta manera, conocer el grupo de tratamiento en el que se encuentra un participante no influye en el participante ni en el equipo del estudio.
Cuando se completan los estudios clínicos, o cuando el enmascaramiento ya no sea necesario, se revela el grupo de tratamiento asignado para cada participante.